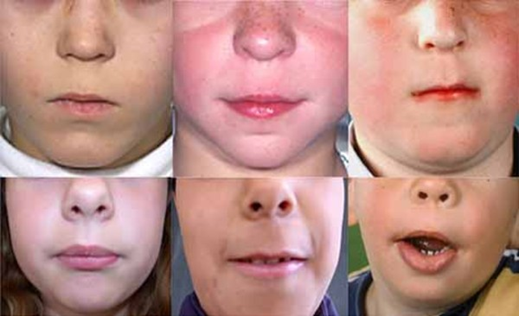
Jeune sendrom öncelikle kemikleri etkileyen nadir bir durumdur. Yaygın belirti ve semptomlar arasında akciğerlerin büyümesini ve genişlemesini kısıtlayan küçük bir göğüs ve kısa kaburgalar bulunur ve bu da genellikle hayatı tehdit eden solunum güçlüklerine neden olur. Diğer semptomlar kollarda ve bacaklarda alışılmadık şekilli kısaltılmış kemikleri içerebilir. Kemikler ve ekstra parmaklar veya ayak parmakları. Bebeklik döneminin nefes alma zorluklarından kurtulan insanlar daha sonra ciddi böbrek veya kalp problemleri geliştirebilir. Birçok durumda Jeune sendromunun nedeni bilinmemektedir; ancak, değişiklikler (mutasyonlar) birkaç farklı genler bu durumdaki bazı ailelerde tanımlanmıştır. Jeune sendromumiras bir otozomal resesiftavır. Tedavi, her insanda mevcut olan belirti ve semptomlara dayanır.
Boğucu torasik distrofi olarak da adlandırılan Jeune sendromu, dar bir toraks, kısa uzuvlar ve asetabula’nın ‘trident’ yönü ve metafiz değişikliklerini içeren radyolojik iskelet anormallikleri ile karakterize kısa bir kaburga displazisidir. Yıllık doğum sıklığı bilinmemektedir ancak 1-5 / 500.000 olduğu tahmin edilmektedir.
Polidaktili olan veya olmayan kısa kaburga torasik displazi (SRTD), dar bir torasik kafes, kısa kaburgalar, kısaltılmış tübüler kemikler ve asetabular çatının ‘trident’ görünümü ile karakterize edilen bir grup otozomal resesif iskelet sililpatisine işaret eder. SRTD, Ellis-van Creveld sendromunu (EVC) ve daha önce Jeune sendrom veya boğucu torakal distrofi (ATD), kısa kaburga-polidaktili sendromu (SRPS) ve Mainzer-Saldino sendromu olarak tanımlanan bozuklukları kapsar.
KROMOZOMAL KONUM
Sitogenetik Yer: 7q36.3, 36.3 konumundaki kromozom 7’nin uzun (q) kolu
Moleküler Yer: Kromozom 7’de baz çiftleri 158.839.245 ila 158.958.695 (Homo sapiens Güncellenmiş Ek Açıklama Bülteni 109.20191205, GRCh38.p13)
BU GENİN DİĞER İSİMLERİ
- CFAP163
- DIC6
- FAP163
- SRPS6
- SRTD8
Jeune Sendromun’un Eş anlamları
- boğucu torasik displazi
- ATD
- torasik-pelvik-falangeal distrofi
- boğucu torasik kondrodistrofi
- kondroektodermal displazi benzeri sendrom
- infantil torasik distrofi
- Jeune torasik distrofisi
Etkilenen Popülasyonlar
ATD insidansı 100.000 ila 200.000 canlı doğumda yaklaşık 1’dir. Erkekler ve dişiler, çeşitli etnik veya ırksal geçmişlere sahip kişiler gibi eşit sayıda etkilenmiş gibi görünmektedir.
Klinik Özellikler
Maroteaux ve Savart (1964) torasik distrofiyi boğucu olarak tanımladılar ve göğüs kafesi, pelvis ve uzuvlardaki iskelet değişikliklerinin Ellis-van Creveld sendromunda (EVC; 225500 ) gözlemlenenlere benzer olduğunu belirttiler . Pirnar ve Neuhauser (1966) etkilenen 3 erkek kardeş bildirmiş ve tırnaklarının displazisi olmadan polidaktili varlığını belirtmiştir. Erken çocukluk döneminde hayatta kalanlar, kronik nefrit ( Wahlers, 1966 ) ve bağırsak malabsorpsiyonu ( Karjoo ve diğerleri, 1973 ) gibi başka bozukluklar geliştirme eğilimindeydi .
Hanissian ve diğ. (1967) her biri 2 erkek kardeşi olan 2 aile bildirmiştir; 1 aile Afrika kökenliydi. Bu yazarlar, Shapira ve ark. (1965) bu duruma sahipti.
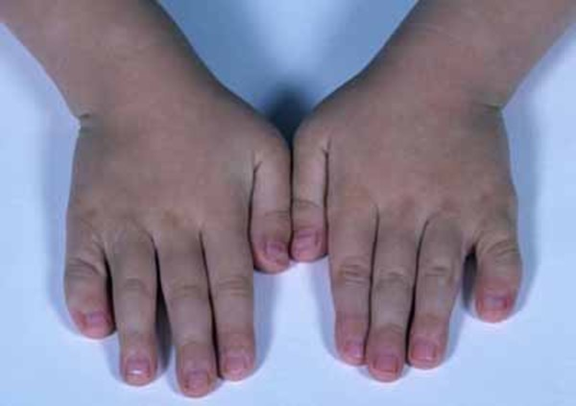
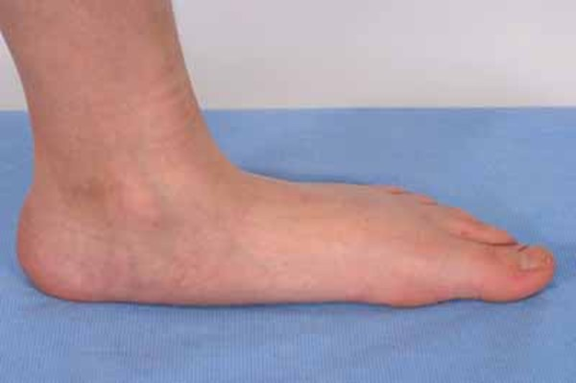
Langer (1968) , polidaktili olgularda, sadece radyolojik nedenlerle Ellis-van Creveld sendromundan farklılaşmanın mümkün olmayabileceğine dikkat çekmiştir. Polidaktili, ATD’nin tutarsız bir özelliğidir ve mevcut olduğunda genellikle ayakları da etkiler. Aksine, ellerin polidaktili EVC’de sabit bir özelliktir, ancak ayaklar nadiren etkilenir. ATD’deki ana viseral anormallik renaldir, oysa EVC’de kardiyaktır.
Shokeir (1970) , Norveç ekstraksiyonunun boğucu torasik distrofisi ile ilişkili 5 etkilenmiş kişiyi tanımlamıştır. Kistik böbrek değişiklikleri (Potter tip IV) tanımlandı. Kistik lezyonlar böbrek, karaciğer ve pankreasta ortaya çıkabilir ( Hopper ve ark., 1979 ; Landing ve ark., 1980 ).
Finegold ve diğ. (1971) hipoplastik akciğerli bir olgu ve otopside alveol sayısında belirgin bir azalma olduğunu bildirmişlerdir.
Oberklaid ve diğ. (1977) 10 vaka bildirmiştir. Böbrek ve karaciğer değişiklikleri progresifti ve en az 2 hastada ölüm nedeni böbrek yetmezliği idi. Dikkate değer bir vaka, hala 15 yaşında ve boy için 25. yüzdelikte yaşayan bir çocuğun vakasıydı. Küçük bir göğsü vardı, ancak tek radyolojik bulgu kısa kaburgalardı. 32 yaşında bir hasta Friedman ve ark. (1975) .
Turkel ve diğ. (1985) otopside 7 yenidoğan vakasını incelemiş; 2’si akraba ebeveynlerinden doğan kardeşlerdi. Cüce telaffuz edilmedi; polidaktili de olan sadece bir bebekte uzuvlar kısaydı. Enkondral ossifikasyon femur, omur ve kaburga bölümlerinde düzensizdi. Pulmoner hipoplazi küçük toraks ile ilişkili idi. Periportal fibroz, safra kanalı proliferasyonu, siroz (1 vakada) ve değişken pankreatik fibroz da tarif edildi.
Whitley ve diğ. (1987) , yenidoğan döneminde direkt hiperbilirubinemi ve hepatik fibroz ile ilişkili karaciğer fonksiyon bozukluğunu tarif etmişlerdir. Hudgins ve diğ. (1990) , sirozla ilişkili progresif hepatik disfonksiyonu olan bu bozukluğa sahip 2 sib tanımlamıştır. Giorgi ve diğ. (1990) , hafif bir sendrom formuna sahip 2 kız kardeş tanımlamıştır.
Zack ve Beighton (1995) akraba çiftli karışık soydan 6 çocuğun 1’inde spondiloenfondromatoz (bkz. 607944 ) adını verdiklerini açıkladılar . İlk olarak 2.5 yaşında görüldüğünde, psödoakondroplazi ( 177170 ) için geçici bir tanı konulmuştur, ancak daha sonra özellikler spondiloenfondromatozun radyolojik görünüm tanısına dönüşmüştür. Gez ile, pelvisin 2.5 yaşında konfigürasyonu, boğucu toraks displazisini bir şekilde düşündürdü. Daha sonra, 13 yaşında çekilen fotoğraflarla belirtildiği gibi, göğsün belirgin daralması gelişti.
Labrune ve diğ. (1999) Jeune sendrom ve karaciğer hastalığı klinik ve laboratuvar bulguları olan 3 çocuk bildirmişlerdir. Karaciğer tutulumu şiddetliydi ve hepatik fibrozise ve daha sonra portal hipertansiyonlu biliyer siroza yol açtı. Bir hastada uzamış neonatal kolestaz ilk tezahürken, diğer 2 hastada fibroz ve hatta siroz geliştiğinde hepatik lezyonlar geç fark edildi. Ursodeoksikolik asit ile tedavinin, klinik ve laboratuvar verilerindeki iyileşmeye bağlı olarak hepatik disfonksiyonun ilerlemesini kontrol ettiği görülmüştür. Yazarlar, serum safra asidi konsantrasyonu ölçümleri de dahil olmak üzere Jeune sendromlu hastalarda hepatik fonksiyonun düzenli olarak takip edilmesi gerektiğini önerdiler.
Kajantie ve diğ. (2001) , yenidoğan semptomları hafif solunum sıkıntısından asfiksi ve ölüme kadar değişen ATD’li 3 sib tarif etmişlerdir. Yazarlar, üçüncü trimesterden önce genç siblerin doğum öncesi tanısında zorluklar olduğunu bildirmişlerdir. Şiddetli etkilenen hastaların bile yeni yenidoğan yoğun bakım tedavi seçenekleri göz önüne alındığında uygun bir prognoza sahip olabileceğini önerdiler.
NORMAL İŞLEVLER
WDR60 geni, WD tekrar protein ailesinin bir üyesini kodlar. WD tekrarları, tipik olarak gl-his ve trp-asp (GH-WD) tarafından desteklenmiş yaklaşık 40 amino asidin minimal olarak korunmuş bölgeleridir ve heterotrimerik veya multiprotein komplekslerinin oluşumunu kolaylaştırabilir. Bu ailenin üyeleri hücre döngüsü ilerlemesi, sinyal iletimi, apoptoz ve gen regülasyonu dahil olmak üzere çeşitli hücresel süreçlerde yer alır. Kodlanmış protein dört WD tekrarı içerir ve silya oluşumunda rol oynayabilir. Bu gendeki mutasyonlar kısa kaburga polidaktili ve Jeune sendromları ile ilişkilendirilmiştir.
GENETİK DEĞİŞİKLERE İLİŞKİN SAĞLIK KOŞULLARI
Polidaktili olan veya olmayan kısa kaburga torasik displazi 8 (SRTD8): Kısa kaburga torasik displazi, bir grup otozomal resesif ciliopati ve daraltılmış torasik kafes, kısa tırtıklı kemikler ile karakterize asetabular çatının görünümü. Polidaktili değişken olarak mevcuttur. İskelet dışı tutulum, yarık dudak / damak yanı sıra beyin, göz, kalp, böbrekler, karaciğer, pankreas, bağırsaklar ve genital organlar gibi ana organların anomalilerini içerebilir. Hastalığın bazı formları yenidoğan döneminde ciddi şekilde kısıtlanmış torasik bir kafese ikincil solunum yetmezliği nedeniyle öldürücüdür, diğerleri ise yaşamla uyumludur. Hastalık spektrumu Ellis-van Creveld sendromunu, boğucu torasik distrofiyi (Jeune sendromu), Mainzer-Saldino sendromunu ve kısa kaburga-polidaktili sendrom
BELİRTİLER
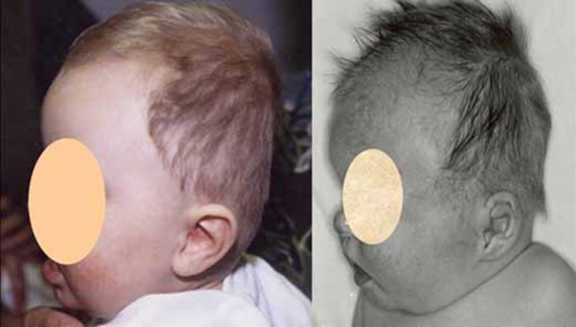
Jeune sendromöncelikle kemikleri etkileyen nadir bir durumdur. Bu durumdan etkilenen insanlar tipik olarak iskelet anormallikleri ile doğarlar:
- Küçük, dar göğüs
- Kısa kaburgalar
- Kolların ve bacakların kısaltılmış kemikleri
- Alışılmadık şekilli pelvis
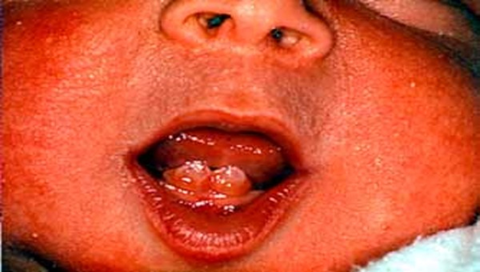
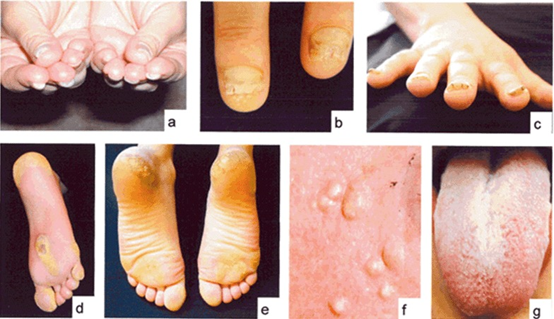
- Ekstra parmaklar ve / veya ayak parmakları
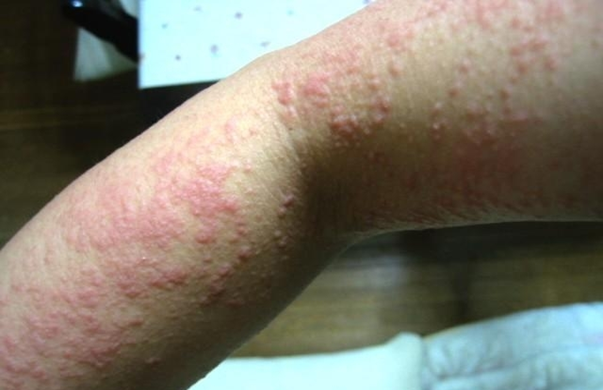
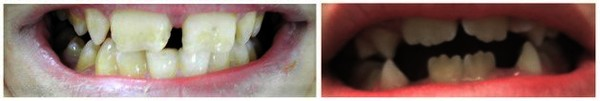
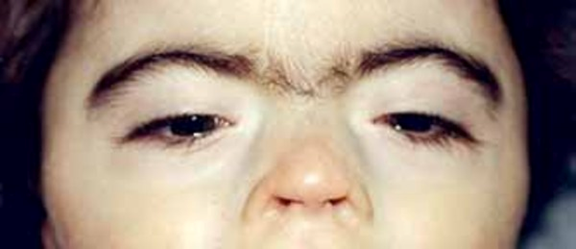
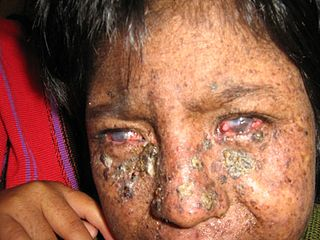
Jeune sendromunun diğer özellikleri şunlardır; yüksek tansiyon, karaciğer hastalığı, pankreas kistleri, diş anormallikleri ve göz hastalığı görme kaybına yol açabilecek retina distrofisi denir.
Hastalar tipik olarak yenidoğan döneminde değişken derecelerde solunum sıkıntısı ve tekrarlayan solunum yolu enfeksiyonları ile başvururlar. Bu solunum problemleri ATD’nin en ciddi komplikasyonlarıdır ve bu hastalarda mortalitenin ana nedenidir. Bazı raporlar ATD’li çocukların% 60-80’inin bebeklik döneminde veya doğumdan sonraki ilk birkaç yıl içinde öldüğünü göstermektedir. Erken çocukluk döneminde yaşayan hastalar için, solunum problemleri yaşla birlikte iyileşme eğilimi gösterir, böylece bir hasta alt grubu ergenlik veya yetişkinliğe yaşayabilir.
Çocuk büyüdükçe ATD’nin diğer komplikasyonları da olabilir: yüksek tansiyon, böbrek kistleri, pankreas kistleri ve daha az yaygın karaciğer hastalıkları, diş anormallikleri ve azalmış veya kötüleşen görme (retinal distrofi).
Etkilenen bireyler, böbrek yetmezliğine veya arızalara neden olabilecek kronik nefrit (böbrek rahatsızlığı) geliştirebilir. Kalp anormallikleri ve hava yolunda daralma da görülebilir.
SEBEPLERİ
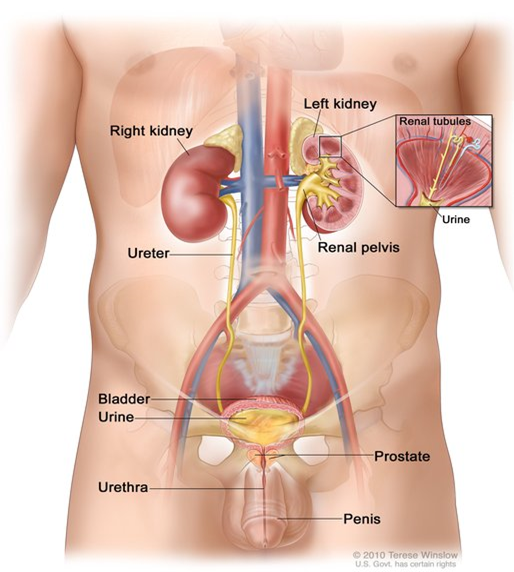
Birçok durumda, Jeune’nin sendrom nedeni bilinmeyen, ancak değişiklikler (mutasyonlar) birkaç farklı genler( IFT80 , DYNC2H1 , WDR19 , IFT140 ve TTC21B ) bu durumdaki bazı ailelerde tanımlanmıştır. Bu genlerin tümü,protein içinde bulunan hücresiliya adı verilen ve hücrelerin yüzeyinde mikroskobik, parmak benzeri çıkıntılar olan yapılar . Kirpilerin gelişimini ve bakımını bozan mutasyonların Jeune sendromu ile ilişkili belirti ve semptomlara nasıl yol açtığı net değildir.
11 gendeki mutasyonların ATD’nin bugüne kadar neden olduğu bulunmuştur. Genler şunlardır: CEP120, CSPP1, DYNC2H1, IFT80, IFT140, IFT172, TTC21B, WDR19, WDR34, WDR35 ve WDR60 . Etkilenen bireylerin yüzde 70’inin bu 11 genden birinde mutasyona sahip olduğu tahmin edilmektedir. Bu genlerdeki mutasyonlar, kemik gelişimini etkileyen anormal kirpikler proteinlerine yol açar.
ATD, otozomal resesif genetik bir hastalık olarak kalıtsaldır. Resesif genetik bozukluklar, bir birey her bir ebeveynden aynı özellik için aynı anormal geni miras aldığında ortaya çıkar. Bir kişi hastalık için bir normal gen ve bir gen alırsa, kişi hastalık için bir taşıyıcı olacaktır, ancak genellikle semptom göstermez. İki taşıyıcı ebeveynin hem değiştirilmiş geni geçmesi hem de etkilenen bir çocuğa sahip olma riski her hamilelikte% 25’tir. Her hamilelikte ebeveyn gibi taşıyıcı olan bir çocuk sahibi olma riski% 50’dir. Bir çocuğun her iki ebeveynten normal gen alma şansı% 25’tir. Risk erkekler ve kadınlar için aynıdır.
TEŞHİS
Bazı durumlarda, Jeune tanısı sendromKarakteristik eğer doğumdan önce şüpheli olabilir belirti ve bulgular mevcut olanultrason. Doğumdan sonra Jeune sendromuRöntgenBulgular. Bazı ailelerde, teşhis ile doğrulanabilirgenetik test.
- Genetik Test Kayıt (GTR) bu durum için genetik testler konusunda bilgi sağlar. GTR için hedef kitle sağlık hizmeti sağlayıcıları ve araştırmacılardır. Genetik test hakkında özel soruları olan hastalar ve tüketiciler bir sağlık uzmanı veya bir genetik uzmanıyla görüşmelidir.
- Orphanet , bu durum için tanısal testler sunan uluslararası laboratuvarları listeler.
TEDAVİ
Tedavi, solunum yolu enfeksiyonlarını yönetmeye ve böbrek ve karaciğer fonksiyonlarını düzenli olarak izlemeye dayanır. Şiddetli solunum yolu enfeksiyonu riski iki yaşından sonra azalır.
Dikey genişletilebilir protez titanyum kaburga (VEPTR), pediyatrik hastalarda torasik yetmezlik sendromunun (TIS) tedavisi için 2004 yılında FDA tarafından onaylanmıştır. TIS, göğüs, omurga ve kaburgaların ciddi deformitelerinin normal nefes almayı ve akciğer gelişimini engellediği konjenital bir durumdur. VEPTR, omurganın düzeltilmesine ve kaburgaların düzleştirilmesine yardımcı olan implante edilmiş, genişletilebilir bir cihazdır, böylece akciğerler büyüyecek ve nefes almak için yeterli hava ile doldurulabilir. Cihazın uzunluğu hasta büyüdükçe ayarlanabilir. Spondilotorasik displazi tedavisi için, göğsün her iki tarafında kaburgalar ayrılır ve göğsün her iki tarafına VEPTR’ler yerleştirilir. Raynham Mass’ta DePuy Synthes Spine Co. tarafından üretilmektedir.
ETOLOJİSİ
Sendromun moleküler temeli, her biri bir intraflagellar taşıma proteinini kodlayan IFT80 (3q25.33), DYNC2H1 (11q22.3), WDR19 (4p14) ve TTC21B (2q24.3) genlerinin dahil olduğunu gösteren kısmen açıklanmıştır. Jeune sendromunun ciliopathies grubuna ait olduğu. Diğer genlerdeki mutasyonlar da hastalığa karışabilir ve tanımlanmaya devam edebilir.
PROGNOZ
Visseral ilişkili hastalıklara bağlı olarak prognoz oldukça değişkendir ve ciddi solunum komplikasyonları riski 2 yaşından sonra azalır.
REFERANSLAR
- https://rarediseases.org/rare-diseases/dystrophy-asphyxiating-thoracic/
- https://rarediseases.org/gard-rare-disease/3049/jeune-syndrome/
- https://ghr.nlm.nih.gov/gene/WDR60#synonyms
- https://www.orpha.net/consor/cgi-bin/Disease_Search.php?lng=EN&data_id=283&Disease_Disease_Search_diseaseGroup=Jeune-syndrome&Disease_Disease_Search_diseaseType=Pat&Disease(s)/group%20of%20diseases=Jeune-syndrome&title=Jeune%20syndrome&search=Disease_Search_Simple
- https://www.omim.org/entry/208500?search=Jeune%20syndrome&highlight=%28syndrome%7Csyndromic%29%20jeune
- https://rarediseases.info.nih.gov/diseases/3049/jeune-syndrome
- https://commons.wikimedia.org/wiki/File:Fibrothorax_chest_x-ray.jpg